内容
主要区别
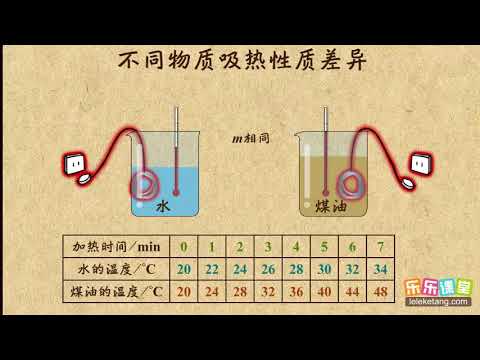
热量是能量的一种形式,当两个物体相互作用时,这种能量很可能从一个物体传递到另一个物体。热能与温度成正比,意味着温度的升高会自动拉动体内热能的增加,反之亦然。这两个术语,即比热和热容量,在热力学中被广泛使用,因为它们均指使物体温度升高所需的能量。比热和热容量彼此非常相似,只是比热的附加变量有所不同。尽管许多人可以互换使用这些术语,因为它们的概念统称为“比热容”。为了获得这两个术语之间的差异,一个人需要了解比热中的其他变量。热容是将物质的温度提高到1摄氏度(°C)或1开尔文,而比热是将质量为1kg或1g的物质的温度提高1摄氏度(°C)或1开尔文。
比较表
| 比热 | 热容量 | |
| 定义 | 比热是使质量为1kg或1g的物质的温度升高1摄氏度(°C)或1开尔文所需的热量。 | 热容是将物质的温度提高到1摄氏度(°C)或1开尔文所需的热量。 |
| 弥撒 | 比热与物体或物质的质量成正比。 | 热容量不取决于质量。 |
| 国际单位 | 公斤-1 ķ-1 | J / K |
什么是比热?
比热与热容非常相似,因为它们都涉及使人体温度升高一个单位,尽管与后者不同,因为它还有一个附加变量,“质量”要在注意的同时注意温度升高一单位。水的比热为4.186 Jg-1oC-1, 用简单的话我们可以说使1增加 Ø在1克水中,C需要4.186焦耳的热能。热量和温度之间的关系可以表示为:
Q =厘米∆T,
哪里,
Q被加热量
C是比热
∆T是温度变化
当遇到相变时,该关系不会保持有效,这意味着将水转换为气态(沸点)或将冰转换为液态(熔点。这是因为在相变过程中除去或添加的热量确实会在理论或实验室工作时,将使用比热而不是热容量,因为它还可以测量物质或物体的质量。
什么是热容?
热容是将物质的温度提高到1摄氏度(°C)或1开尔文所需的热量。吸入的热量或温度的升高与物质的质量无关。热能与温度成正比,意味着温度的升高会自动拉动体内热能的增加,反之亦然。可以使用以下公式定义热容量:
C =ΔQ/ΔT,
哪里,
ΔQ是添加的热量
C是特定的HEAT
ΔT是温度变化
比热与热容量
- 热容是将物质的温度升高到1摄氏度(°C)或1开尔文所需的热量,而比热是将物质1kg或1g的物质的温度升高1度所需的热量。摄氏(°C)或1开尔文。
- 比热与物体或物质的质量成正比,而热容量与质量无关。
- J / K是热容量的SI单位,而J kg-1 ķ-1 是比热的国际单位制。